Cette phrase, tirée d’un conte célèbre, résume une découverte récente d’un groupe de chercheurs d’Université Paris Cité travaillant à l’Institut Cochin et à l’Institut Necker, et qui s’intéresse aux mécanismes moléculaires de l’interaction du méningocoque avec des récepteurs portés par les cellules endothéliales qui tapissent les vaisseaux. Leur étude a été publiée dans Nature Communications le 18 octobre 2019.
© Epictura Pix5
Le méningocoque est une bactérie Gram négative responsable de la méningite cérébrospinale, une infection grave de l’enveloppe du cerveau qui peut s’associer à un choc septique souvent mortel, le « purpura fulminans ». Cette bactérie se caractérise par des organelles particulières, filiformes, appelées pili, qui lui permettent d’interagir avec les cellules endothéliales.
Après plusieurs années de recherche il a été établi que le méningocoque interagissait successivement avec deux récepteurs. Le premier, appelé CD147, est un récepteur permettant l’adhésion de la bactérie aux cellules endothéliales, le second est le récepteur de l’adrénaline, connu sous le nom de récepteur β2-adrénergique. Les signaux cellulaires consécutifs à la fixation du méningocoque sur ce récepteur sont nécessaires à la stabilisation des colonies à la surface des cellules endothéliales et à l’infection des tissus.
Le récepteur β2-adrénergique est un senseur de molécules chimiques (l’adrénaline, en particulier) qui se lient dans une poche du récepteur déclenchant son activation. L‘étude actuelle montre que le méningocoque active ce même récepteur en « tirant dessus ». La force activant le récepteur est générée à la fois par un petit moteur moléculaire qui se trouve à la base des pili de la bactérie et par la force du flux sanguin qui pousse les bactéries adhérant aux vaisseaux. Le second volet de la découverte est que les pili n’interagissent pas avec la charpente protéique du récepteur, comme on aurait pu s’attendre, mais avec des sucres branchés sur son extrémité N-terminale. Il faut que deux chaines sucrées soient à une distance particulière et qu’elles soient terminées par un acide sialique. Ainsi, un récepteur de la même famille que le récepteur β2-adrénergique, mais qui n’est pas activable par le méningocoque le devient si on arrive à lui brancher ces chaines sucrées par génie génétique. Cerise sur le gâteau, cette découverte explique aussi la spécificité d’espèce du méningocoque qui n’infecte que l’homme. En effet, l’acide sialique humain diffère de celui des autres animaux en raison de la perte évolutive d’une enzyme il y a environ 3 millions d’années. Cette perte, sans doute sélectionnée par la résistance qu’elle entraine vis-à-vis d’un parasite, a rendu l’espèce humaine sensible au méningocoque qui s’est adapté à lui spécifiquement. Heureusement, la relative rareté de l’infection par le méningocoque explique son peu d’incidence sur le développement de notre espèce.
Ces informations ouvrent de nouvelles perspectives thérapeutiques de l’infection méningococcique, mais surtout (nous disposons déjà d’antibiotiques très efficaces contre le méningocoque) d’immenses perspectives de recherche sur les différents mécanismes et les effets physiologiques de l’activation mécanique de cette famille de récepteurs.
À lire aussi
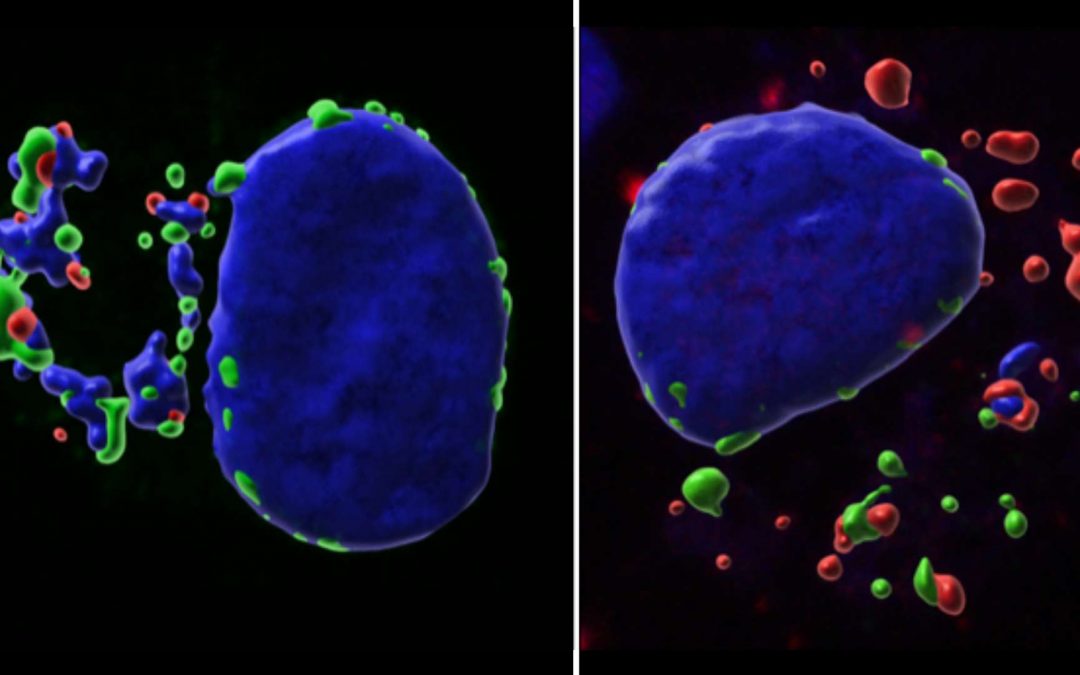
Theileria annulata et Cancer : une stratégie du parasite dévoilée !
L’équipe de recherche du Pr Jonathan Weitzman a mis en lumière le mécanisme par lequel le parasite Theileria annulata, responsable de maladies semblables aux cancers chez les bovins, échappe au mécanisme de défense de la cellule hôte.

Université Paris Cité félicite le professeur Anton Zorich pour l’obtention de son ERC Advanced Grant
ERC Advanced Grant 2023 : le professeur Anton Zorich, mathématicien à l’université Paris Cité compte parmi les 37 lauréates et lauréats français.

Le Deeptech Tour 2024 arrive à Paris !
Créer des ponts entre le monde de l’entrepreneuriat et celui de la recherche, c’est le rôle du Deeptech Tour. Organisée par Bpifrance, cette tournée des campus français vise à réunir l’écosystème universitaire, les acteurs économiques locaux et les structures...

Résultats de l’appel à candidatures 2024 Paris-Oxford Partnership (POP)
Le Comité d’évaluation Paris-Oxford Partnership (POP) de l’université Paris Cité, le CNRS, l’Institut des Etudes Avancées et l’Université d’Oxford, annoncent les résultats de l’AAP visant à faciliter et renforcer les échanges scientifiques entre Paris et Oxford pour...
