L’hyperaldostéronisme primaire est la forme la plus commune d’hypertension artérielle secondaire. Son diagnostic précoce a un impact important sur l’issue thérapeutique. Les travaux de chercheurs de l’Inserm et de l’Université Paris Cité au Paris Centre de recherche Cardiovasculaire (PARCC) de l’Hôpital Européen Georges Pompidou, en collaboration avec des équipes de l’Université Queen Mary à Londres (Royaume Uni) et de l’Université nationale de Malaisie à Kuala Lumpur (Malaisie), ont découvert des anomalies génétiques tout à fait particulières chez des patients développant un hyperaldostéronisme primaire à la puberté, pendant la grossesse ou autour de la ménopause.
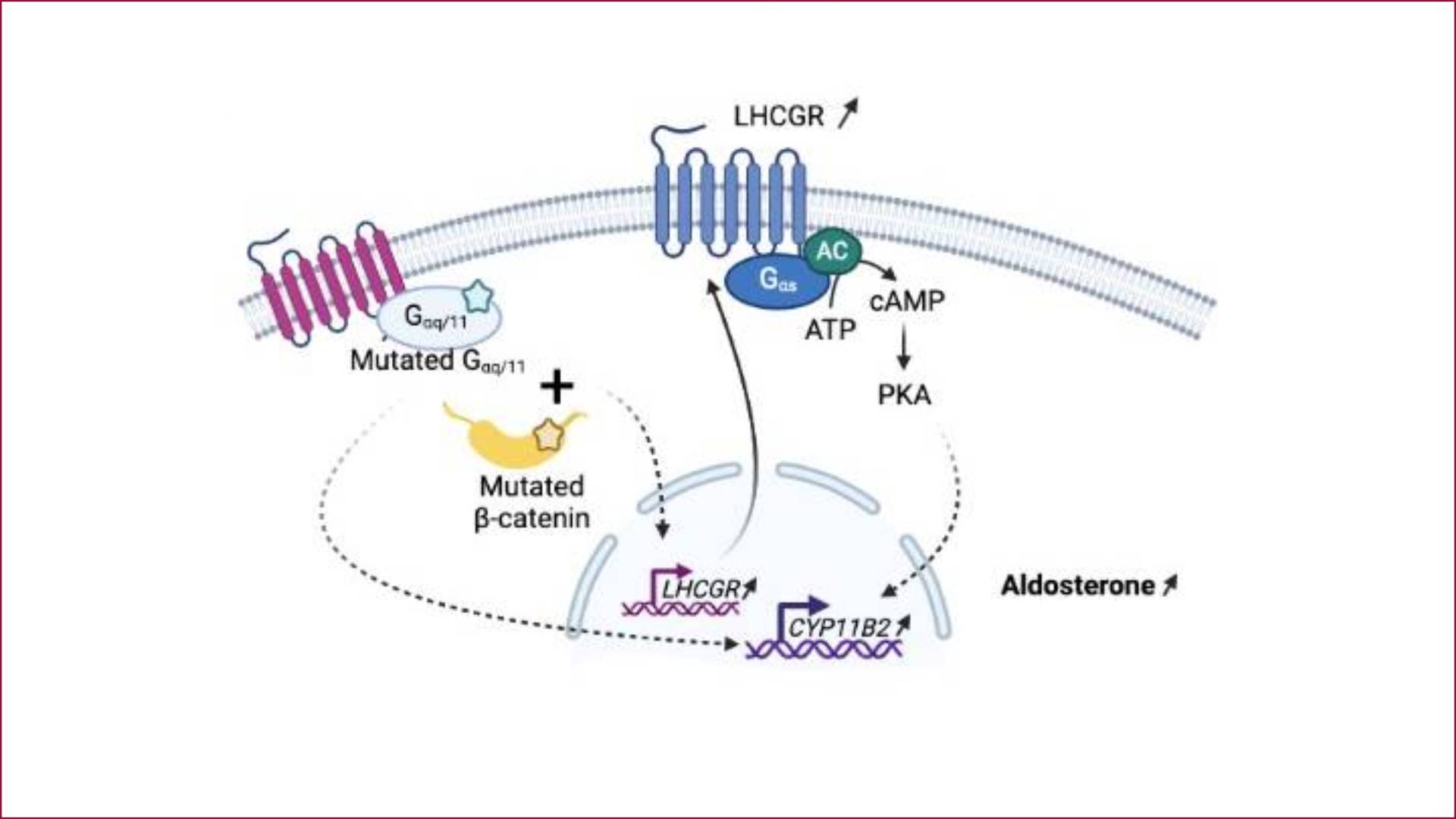
Schéma simplifié des conséquences, dans un adénome produisant de l’aldostérone, de la présence à la fois d’une mutation de la b-catenine et des sous-unités G alpha-11 ou G alpha-q. L’augmentation de l’expression de LHCGR (récepteur à la LH et à l’HCG) pourrait expliquer le développement de l’hyperaldostéronisme à la puberté, pendant la grossesse ou autour de la ménopause.
Ces travaux suggèrent qu’il faut rechercher un hyperaldostéronisme primaire chez des patients présentant une hypertension artérielle notamment pendant la puberté et la grossesse, permettant ainsi un diagnostic rapide et la proposition d’un traitement curatif par ablation de la surrénale atteinte.
L’hypertension artérielle est un facteur de risque cardiovasculaire majeur. Bien qu’il existe un large arsenal thérapeutique, le contrôle optimal de la pression artérielle n’est pas atteint chez quasiment deux tiers des patients. L’identification des formes secondaires d’hypertension artérielle est essentielle pour une meilleure prise en charge des patients hypertendus et la prévention des complications cardiovasculaires.
L’hyperaldostéronisme primaire est la forme la plus commune d’hypertension artérielle secondaire avec une prévalence e 6 à 20% des patients hypertendus. Les adénomes produisant de l’aldostérone et l’hyperplasie bilatérales des surrénales sont responsables de la quasi-totalité des cas d’hyperaldostéronisme primaire. Le diagnostic précoce d’hyperaldostéronisme primaire a un impact très important sur l’issue thérapeutique et la survie, étant donné les effets cardiovasculaires délétères propres à l’excès d’aldostérone. Les conséquences à long terme incluent une augmentation du risque d’infarctus du myocarde, d’accident vasculaire cérébral et de fibrillation auriculaire.
Ces dernières années des avancées majeures ont été faites dans la compréhension des bases génétiques de l’hyperaldostéronisme primaire avec l’identification de mutations somatiques récurrentes dans les adénomes produisant l’aldostérone, touchant des gènes codant pour des canaux ioniques et des ATPases qui régulent l’homéostasie ionique intracellulaire et le potentiel de membrane.
La nouvelle étude menée par les chercheurs Inserm Maria-Christina Zennaro, Sheerazed Boulkroun et Fabio Luiz Fernandes-Rosa au PARCC (Inserm/Université Paris Cité), en collaboration avec des équipes de l’Université Queen Mary au Royaume Uni, de l’Université Nationale de Malaisie et de l’Université d’Uppsala en Suède s’est intéressée aux mécanismes sous-jacents à la manifestation d’un hyperaldostéronisme au moment de la puberté, de la grossesse ou de la ménopause.
Dans ce travail, les chercheuses et chercheurs ont réalisées un séquençage d’exome entier à partir de 41 adénomes produisant de l’aldostérone afin d’identifier les altérations génétiques responsables du développement de l’hyperaldostéronisme primaire. L’idée était d’identifier d’éventuelles nouvelles altérations génétiques impliquées dans cette pathologie pouvant être associées à une présentation clinique ou biochimique particulière.
Ils ont ainsi dans un premier temps identifié, dans 3 tumeurs, d’une part une mutation du gène CTNNB1 qui code pour la b-catenine et d’autre part une mutation dans le gène GNA11 qui code pour la protéine G alpha-11, une sous-unité des protéines G liant la guanine. Parmi les 27 tumeurs porteuses d’une mutation du gène CTNNB1 des cohortes de patients anglais/irlandais, français et suédois, 16 étaient porteuses d’une mutation du gène GNA11 ou de son homologue GNAQ. De façon intéressante, parmi les 16 patients 15 étaient des femmes chez qui l’hyperaldostéronisme primaire avaient été diagnostiqué à la puberté, lors d’une grossesse ou de la ménopause ; le 16ème patient était un jeune garçon pubère.
Ils ont ensuite montré que la présence de ces mutations résultait en une augmentation de la production d’aldostérone et était associée à un profil d’expression génique particulier avec, de façon remarquable, une augmentation de l’expression du récepteur à la LH (hormone lutéinisante) et à l’HCG (hormone Chorionique Gonadotrope), LHCGR, profil pouvant expliquer l’apparition des adénomes lors de pics hormonaux de LH ou HCG.
Les implications cliniques de ces travaux sont importantes puisqu’ils suggèrent fortement qu’il faut rechercher un hyperaldostéronisme primaire chez des patients jeunes présentant une hypertension artérielle pendant la puberté ou la grossesse, permettant ainsi un diagnostic rapide et la proposition d’un traitement curatif par ablation de la surrénale atteinte.
Références
Somatic mutations of GNA11 and GNAQ in CTNNB1-mutant aldosterone-producing adenomas presenting in puberty, pregnancy or menopause – Zhou, J. et al. Nature Genetics, September 2021
DOI: 10.1038/s41588-021-00906-y
À lire aussi

Cochrane France : un engagement renforcé pour la santé fondée sur les preuves
Centre francophone du réseau international Cochrane, Cochrane France œuvre au développement et à la diffusion des données probantes pour éclairer les décisions en santé. Placé sous la direction du Pr Isabelle Boutron, le centre poursuit son engagement scientifique...

Summers Schools 2026 : une expérience internationale d’excellence à l’UFR de Médecine
Cet été l’UFR de Médecine de l’Université Paris Cité ouvrira pour la première fois à des étudiants du monde entier des programmes intensifs d’apprentissage et d’échanges, organisés entièrement en anglais et ouverts à une audience internationale. Pendant deux semaines,...
![[Keynote recherche] Florence Niedergang – Macrophages, virus et bactéries : qui manipule qui ?](https://u-paris.fr/sante/wp-content/uploads/sites/19/2026/02/3d-abstract-medical-background-with-close-up-virus-cells1.jpg)
[Keynote recherche] Florence Niedergang – Macrophages, virus et bactéries : qui manipule qui ?
Florence Niedergang est directrice de l’Institut Cochin et directrice de recherche au CNRS. Elle dirige l’équipe Biologie des phagocytes, infection et immunité, dont les travaux portent sur les interactions hôte–pathogènes, en particulier les mécanismes...
Vers une école de chirurgie d’excellence : le Campus chirurgical du Grand Paris
Ancré sur le site historique de l’ancien hôpital Broussais dans le 14ᵉ arrondissement, le Campus chirurgical du Grand Paris incarne un tournant majeur pour la formation, la recherche et l’innovation en chirurgie. Cette nouvelle École de Chirurgie, fruit d’une...
