Immunothérapie et cancer : la découverte d’un biomarqueur soluble dans le sang fait avancer la thérapie personnalisée
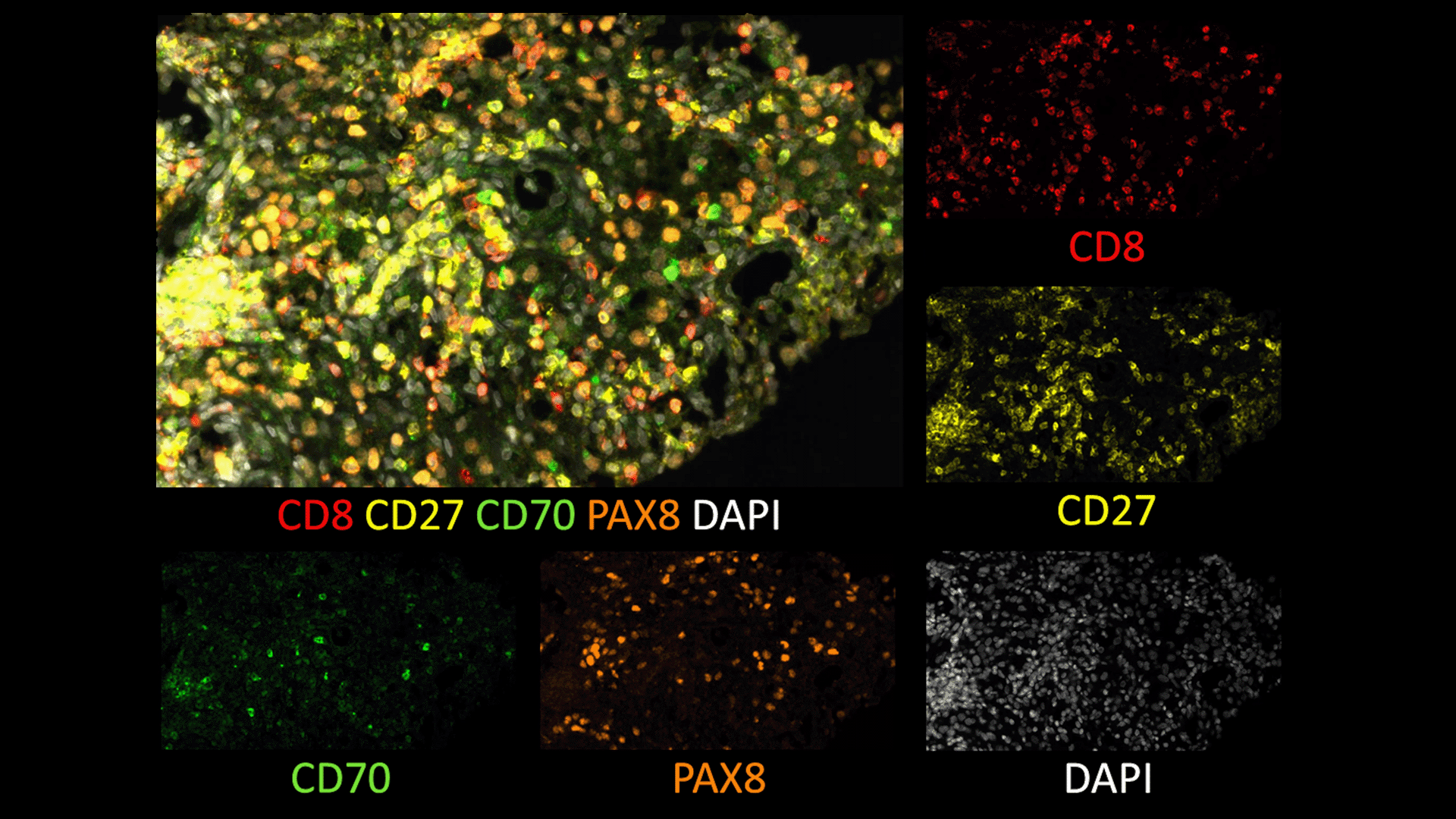
© Professeur Eric Tartour – Université Paris Cité
Interaction entre une cellule tumorale exprimant CD70 et un lymphocyte T-CD27 à partir d’une biopsie d’un patient atteint de cancer du rein
En moins de dix ans, l’immunothérapie a considérablement progressé au point de constituer aujourd’hui une indication thérapeutique dans plus d’une vingtaine de cancers. L’équipe de recherche dirigée par le Pr Eric Tartour, au PARCC (UMR-S 970 Université Paris Cité, Inserm, Hôpital Européen Georges Pompidou – AP-HP), conduit ses recherches en immunothérapie sur le cancer du rein. Dans ses récents travaux, l’équipe a mis en évidence, non seulement l’existence d’un mécanisme qui permet à certaines cellules tumorales dérivées du cancer du rein de survivre à l’action du système immunitaire mais également l’existence d’un biomarqueur soluble dans le sang, CD27, caractéristique de certaines formes de cancer. Ces travaux ont été publiés dans la revue Clinical Cancer Research et ont donné lieu au dépôt de 2 brevets.
Ces dix dernières années la recherche a permis de grandes avancées dans le domaine de l’immunothérapie[1] au point que cette approche complète aujourd’hui l’arsenal thérapeutique disponible en cancérologie dans plus d’une vingtaine de cancer. Pour preuve, seul ou associé à un traitement anti-angiogénique, l’immunothérapie est désormais le traitement de première ligne dans le cas de cancer du rein.
L’équipe de recherche dirigée par le Pr E. Tartour s’intéresse au cancer du rein qui est particulièrement sensible à l’immunothérapie. Aujourd’hui, plusieurs traitements d’immunothérapie sont disponibles pour ce cancer mais encore faut-il pouvoir personnaliser le traitement en proposant celui le plus adapté à chaque forme de cancer. Pour cela, il est indispensable de caractériser de façon approfondie la cellule tumorale et son microenvironnement, composé en partie de cellules immunitaires. Cette identification passe par celle d’un ou plusieurs biomarqueurs (protéine, gène, mutation dans un gène…) spécifiques et donc caractéristiques de chaque forme de cancer. La plupart des biomarqueurs sont identifiés à partir de biopsies réalisées dans la tumeur, ce qui reste un acte médical invasif. L’équipe du Pr E. Tartour, a justement cherché à identifier des biomarqueurs détectables dans le sang grâce à une simple prise de sang et ce, à un stade le plus précoce possible de la maladie.
L’équipe a montré que, dans la tumeur du rein, les cellules tumorales étaient au contact de certaines cellules immunitaires ce qui inhibait la fonction de ces dernières et constituait donc un mécanisme d’échappement de la tumeur au système immunitaire. Plus précisément, ils ont mis en évidence la présence dans les cellules tumorales d’une molécule, CD70, qui se lie avec une molécule, CD27, présente sur les cellules immunitaires et particulièrement les lymphocytes T. Quand cette interaction se met en place les lymphocytes T meurent par apoptose (mécanisme de mort cellulaire) et donc le système immunitaire n’agit plus contre la tumeur.
En mourant, les lymphocytes T libèrent la molécule CD27 sous forme soluble dans le sang. L’équipe du Pr E. Tartour a démontré qu’il y avait un lien étroit entre la présence de CD27 soluble dans le sang et l’interaction entre les cellules tumorales et les lymphocytes T. Elle a également démontré, de manière rétrospective grâce à l’étude de cohortes de biopsies de tumeurs et de plasmas humains, que la présence de CD27 soluble à des taux élevés dans le sang était associée à une mauvaise réponse des patients à l’immunothérapie puisque leurs lymphocytes T, cibles de l’immunothérapie, sont mourants. Ces résultats, publiés dans la revue Clinical Cancer Research ont donné lieu au dépôt d’un 1er brevet.
Désormais l’équipe s’intéresse au mécanisme amont d’interaction entre CD27 et CD70, interaction délétère puisqu’à l’origine de la mort des lymphocytes T et donc de l’inhibition du système immunitaire. Pourquoi ne pas tenter de bloquer cette interaction par une thérapeutique adaptée ? Tel est le questionnement au cœur de leurs travaux pré-cliniques en cours et qui ont, eux aussi, donné lieu au dépôt d’un 2e brevet.
Le Pr E. Tartour se réjouit que ce projet de recherche translationnelle avec des applications cliniques réelles ait été co-porté par Université Paris Cité et l’Inserm transfert, ce qui a permis de bénéficier d’un financement IdEx dans le cadre de l’appel à manifestation d’intérêt (AMI) « Pré-Maturation » d’Université Paris Cité. Cet AMI vise à accompagner les acteurs de la recherche dans leurs projets de transfert technologique et de propriété intellectuelle à valeur marchande vers le monde socio-économique. Ce travail a également bénéficié de l’aide de la plateforme « Cytometry andBiomarkers UtechS » de l’Institut Pasteur.
L’ensemble des travaux et résultats déjà obtenus pourraient intéresser d’autres types de cancers dont les tumeurs expriment, elles aussi, la molécule CD70. Désormais, l’équipe va travailler avec un industriel pour les prochains essais cliniques de façon à tester, de façon prospective, le biomarqueur pour ensuite pouvoir proposer le traitement le mieux adapté au patient selon la forme de cancer qu’il développe.
[1] L’immunothérapie consiste à stimuler, par diverses techniques, le système immunitaire du patient pour que l’organisme se défende seul et ainsi éviter, lorsque c’est possible, de recourir à des traitements lourds aux effets secondaires notables comme la chimiothérapie.
Références
Plasma CD27, a surrogate of the intratumoral CD27-CD70 interaction, correlates with immunotherapy resistance in renal cell carcinoma
DOI : https://doi.org/10.1158/1078-0432.CCR-22-0905
Contact presse
presse@u-paris.fr
-
Nadine Benhamouda, technicienne, responsable de la plateforme mixte Hôpital Européen Georges Pompidou (HEGP) -Hôpital Necker de l’APHP et membre de l’équipe « Immunothérapie et traitement anti-angiogénique en cancérologie » UMR-S 970 (Université Paris Cité, Inserm, Hôpital Européen Georges Pompidou – AP-HP). Elle a bénéficié d’une subvention du DMU Biophygen.
-
Ikuan Sam, Doctorante dans l’équipe Immunothérapie et traitement anti-angiogénique en cancérologie UMR-S 970 (Université Paris Cité, Inserm, Hôpital Européen Georges Pompidou – AP-HP)
-
Stéphane Oudard, Chef du Service d’Oncologie Médicale de l’HEGP et membre de l’équipe « Immunothérapie et traitement anti-angiogénique en cancérologie » UMR-S 970 (Université Paris Cité, Inserm, Hôpital Européen Georges Pompidou – AP-HP)
-
Eric Tartour, PU-PH à Université Paris Cité, directeur de l’équipe Immunothérapie et traitement anti-angiogénique en cancérologie UMR-S 970(Université Paris Cité, Inserm, Hôpital Européen Georges Pompidou – AP-HP) et Chef du service d’immunologie biologique de l’hôpital Européen Georges Pompidou et Hôpital Necker
À lire aussi
Bioprothèses valvulaires cardiaques : un mécanisme clé identifié pour expliquer leur compatibilité avec le sang et leur résistance à la calcification
Les bioprothèses valvulaires cardiaques sont aujourd’hui largement utilisées en chirurgie pour remplacer des valves cardiaques défaillantes. Dans une nouvelle étude, une équipe de recherche de l’Université Paris Cité, de l’Inserm et de l’AP-HP coordonnée par le Pr....

Plan Quantique de l’Université Paris Cité : une approche structurée de la recherche, de la formation et de l’innovation
Les technologies quantiques constituent aujourd’hui un domaine scientifique majeur dans lequel l’Université Paris Cité s’implique activement en conduisant des actions de recherche et de formation de manière structurée et complémentaire autour de son plan quantique....

Rencontrez l’Université Paris Cité au salon Global Industrie
Dans un contexte de transformations scientifiques et technologiques accélérées, l’Université Paris Cité place l’innovation au cœur de sa stratégie. Productrice de connaissances, l’université est aussi un acteur clé du développement industriel, de la compétitivité des...

Une espèce d’abeille européenne sur dix menacée : une nouvelle alerte pour la biodiversité
La nouvelle liste rouge européenne des abeilles, publiée le 26 février 2026, recense près de 2000 espèces et dresse un constat préoccupant : 172 espèces en Europe sont aujourd’hui menacées d’extinction. Dix ans après une première évaluation partielle, l’état des...
