Le virus SARS-CoV-2, responsable de la Covid-19, peut provoquer un syndrome respiratoire aigu sévère, mais avant son apparition en 2019, d’autres coronavirus étaient déjà connus pour être responsables de rhumes saisonniers bénins. Pour quelles raisons un coronavirus va-t-il affecter plus sévèrement l’humain qu’un autre coronavirus ? Les chercheuses et chercheurs de l’Institut Pasteur, d’Université Paris Cité et du VRI apportent aujourd’hui un élément de réponse en identifiant la porte d’entrée d’un coronavirus saisonnier, le virus HKU1, dans les cellules humaines. Le récepteur sur lequel se fixe le HKU1 est différent de celui utilisé par le SARS-CoV-2, ce qui pourrait expliquer en partie la différence de sévérité de ces deux coronavirus.
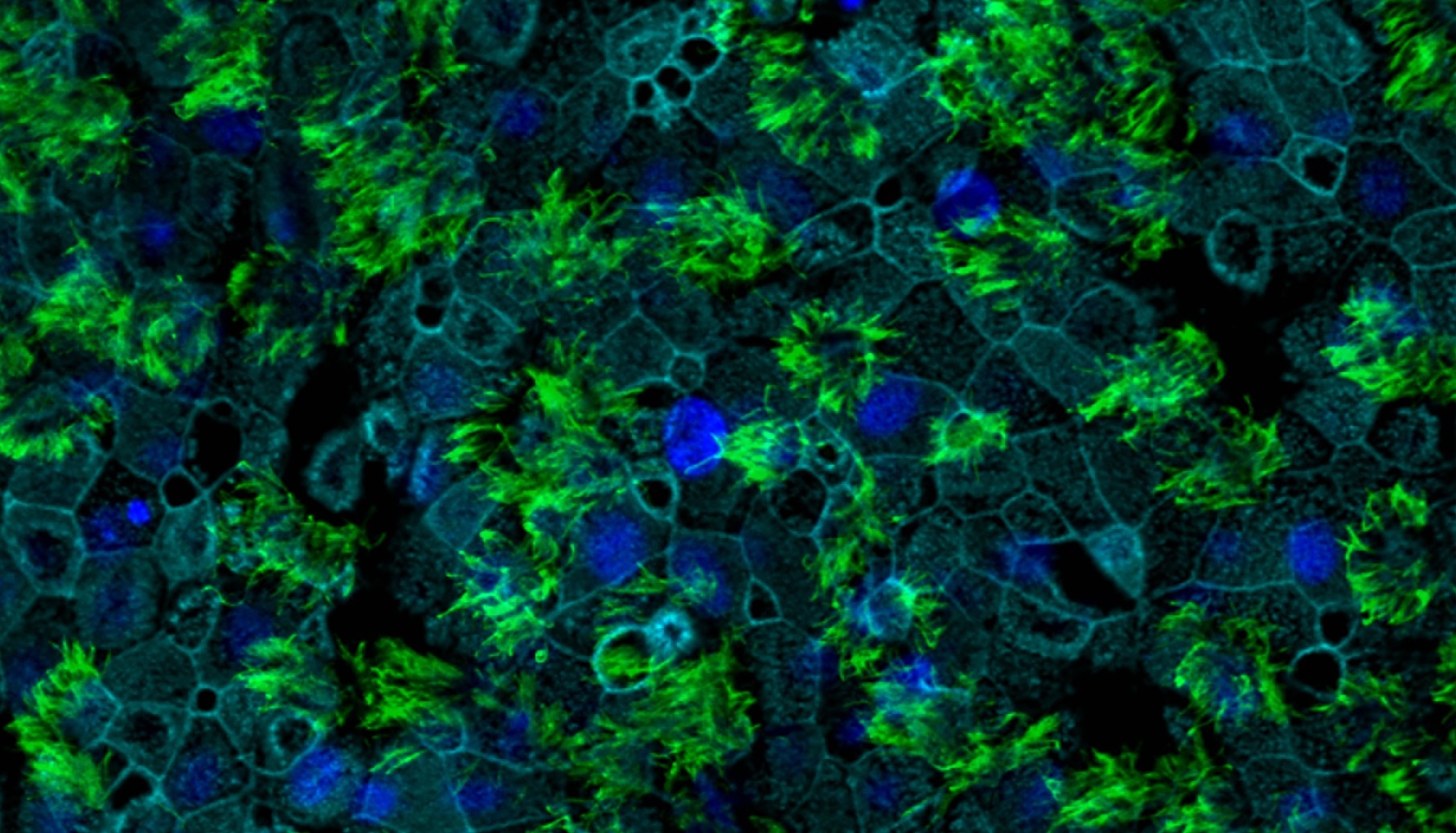
Tissu respiratoire humain, avec les cellules ciliées marquées en vert (anticorps anti-TMPRSS2), noyaux en bleu foncé, membranes cellulaires en bleu clair.
© Vincent Michel, Institut Pasteur
Sept coronavirus sont connus pour avoir la capacité d’infecter les humains. Quatre sont généralement bénins : HKU1, 229E, NL63 et OC43, et trois sont plus pathogènes : SARS-CoV-1, Mers-CoV et SARS-CoV-2.
Le virus HKU1 a été identifié pour la première fois chez un patient âgé atteint d’une pneumonie grave à Hong Kong en 2005. Le HKU1 infecte essentiellement les cellules de l’arbre respiratoire supérieur, comme le SARS-CoV-2, mais il atteint rarement les bronches et alvéoles pulmonaires. Le virus HKU1 provoque des rhumes et autres symptômes respiratoires bénins. Des complications incluant de graves infections des voies respiratoires, en particulier chez les jeunes enfants, les personnes âgées et les personnes immunodéprimées peuvent survenir. On estime que 70 % des enfants sont infectés avant l’âge de 6 ans. Au total, entre 75 et 95 % de la population mondiale a été exposée au HKU1, de manière comparable aux autres coronavirus humains saisonniers.
Au niveau cellulaire, après s’être liées à leurs récepteurs, les protéines de spike des coronavirus sont clivées, c’est-à-dire scindées en deux parties. Ce phénomène de clivage est indispensable pour la fusion du virus, l’entrée et la multiplication virale. Certains coronavirus (SARS-CoV-2 et NL63) utilisent le récepteur ACE2 comme porte d’entrée dans les cellules. Les seuls coronavirus dont les récepteurs n’étaient pas connus jusqu’à présent sont HKU1 et OC43.
Les scientifiques de huit unités de l’Institut Pasteur ont collaboré et identifié l’enzyme TMPRSS2 comme étant le récepteur sur lequel HKU1 se fixe pour entrer dans les cellules. Après cette liaison, TMPRSS2 déclenche la fusion de HKU1 avec la cellule et entraîne ainsi l’infection virale. Les chercheuses et chercheurs montrent, par une combinaison de techniques in vitro et en culture cellulaire, que TMPRSS2 est un récepteur de haute affinité pour la spike de HKU1, ce qui n’est pas le cas pour SARS-CoV-2.
« Identifier le récepteur d’un virus permet de mieux caractériser les cellules ciblées, de comprendre les mécanismes d’entrée et de multiplication virale ainsi que la physiopathologie de l’infection, » commente Olivier Schwartz, co-principal auteur de l’étude et directeur de l’unité Virus et immunité à l’Institut Pasteur.
« Nos résultats illustrent aussi les diverses stratégies d’évolution des coronavirus, qui utilisent TMPRSS2 soit pour se lier aux cellules cibles, soit pour amorcer la fusion et l’entrée virale, » complète Julian Buchrieser, co-principal auteur de l’étude et chercheur au sein de l’unité Virus et immunité à l’Institut Pasteur.
L’utilisation de différents récepteurs impacte probablement le degré de sévérité de ces virus pathogènes pour l’homme. En effet, la présence des récepteurs varie entre les cellules de l’arbre respiratoire et va donc influencer la sensibilité des cellules à l’infection, et la propagation virale. Connaître la voie d’entrée cellulaire devrait permettre aussi de mieux lutter contre l’infection à travers le développement de thérapies ciblées, et d’évaluer le risque de virulence des prochains coronavirus qui pourraient émerger.
En parallèle, les équipes de l’Institut Pasteur menées par Pierre Lafaye et Felix Rey ont développé et caractérisé des nano-anticorps (tout petits anticorps) qui bloquent l’infection par le HKU1 en se fixant sur le récepteur TMPRSS2. Ces réactifs ont été brevetés pour de potentielles activités thérapeutiques.
Ces travaux ont été financés par les organismes de recherche cités plus haut, ainsi que par La Fondation pour la Recherche Médicale (FRM), l’ANRS-MIE, le Vaccine Research Institute, le projet européen HERA DURABLE, le Labex IBEID, et le projet ANR/FRM Flash Covid.
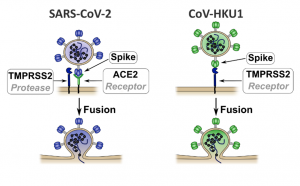
Différentes voies d’entrée du SARS-CoV-2 et de HKU1 dans les cellules humaines. SARS-CoV-2 se fixe sur la protéine ACE2. La protéase TMPRSS2 coupe ensuite la spike pour permettre la fusion du virus et l’entrée dans la cellule cible. HKU1 se fixe directement sur TMPRSS2 pour entrer dans la cellule sans utiliser ACE2. © Institut Pasteur
Références
TMPRSS2 is a functional receptor for human coronavirus HKU1, Nature, 25 octobre 2023
DOI :
À lire aussi

La semaine du cerveau 2026 à l’Université Paris Cité

Prix Jeunes Talents France L’Oréal-UNESCO Pour les Femmes et la Science : Appel à candidatures 2026
La Fondation L'Oréal, en partenariat avec la Commission nationale française pour l'UNESCO et l'Académie des sciences, déclare officiellement ouvert l'appel à candidatures de l'édition 2026 du Prix Jeunes Talents France L'Oréal-UNESCO Pour les Femmes et la Science :...

Suivi des maladies chroniques : un patient sur deux serait ouvert à la téléconsultation
L’étude REACTIVE, coordonnée par la Dre Tiphaine Lenfant et le Pr Viet-Thi Tran et menée par des équipes de médecine interne de l’hôpital européen Georges-Pompidou AP-HP, du centre d’épidémiologie clinique de l’hôpital Hôtel-Dieu AP-HP, de l’Université Paris Cité, de...

Le Collège de l’Académie nationale de médecine : une première promotion marquée par l’engagement de l’Université Paris Cité
Créé en décembre 2023, le Collège de l’Académie nationale de médecine se veut être un lieu d’échanges entre les académiciens et des jeunes médecins, chirurgiens, biologistes, scientifiques, pharmaciens, vétérinaires. Il réunit ainsi 38 jeunes scientifiques, dont 15...
