Une équipe de chercheurs et de médecins des services de cardiologie et maladie vasculaire et d’anesthésie réanimation de l’hôpital Européen Georges-Pompidou AP-HP, d’Université Paris Cité et de l’Inserm, a réalisé une étude clinique (la première réalisée sur l’homme) pour évaluer la sécurité, la faisabilité et les performances de l’appareil Valvosoft.
La morbidité et les complications associées au remplacement chirurgical et transcathéter de la valve aortique calcifiée (SAVR/TAVR) restent élevées. En outre, certains patients ne sont pas éligibles pour ces traitements invasifs. Cardiawave© (co-fondé par le Pr Emmanuel Messas, spinoff d’une collaboration entre l’hôpital Européen Georges-Pompidou AP-HP et les laboratoires Physique pour la médecine (Unité Mixte de Recherche de l’INSERM, de l’ESPCI Paris, de La Pitié-Salpêtrière AP-HP et du CNRS) et Institut Langevin (Unité Mixte de Recherche de l’ESPCI Paris et du CNRS) a mis au point un nouveau dispositif non invasif de thérapie par ultrasons appelé Valvosoft pour traiter la sténose aortique.
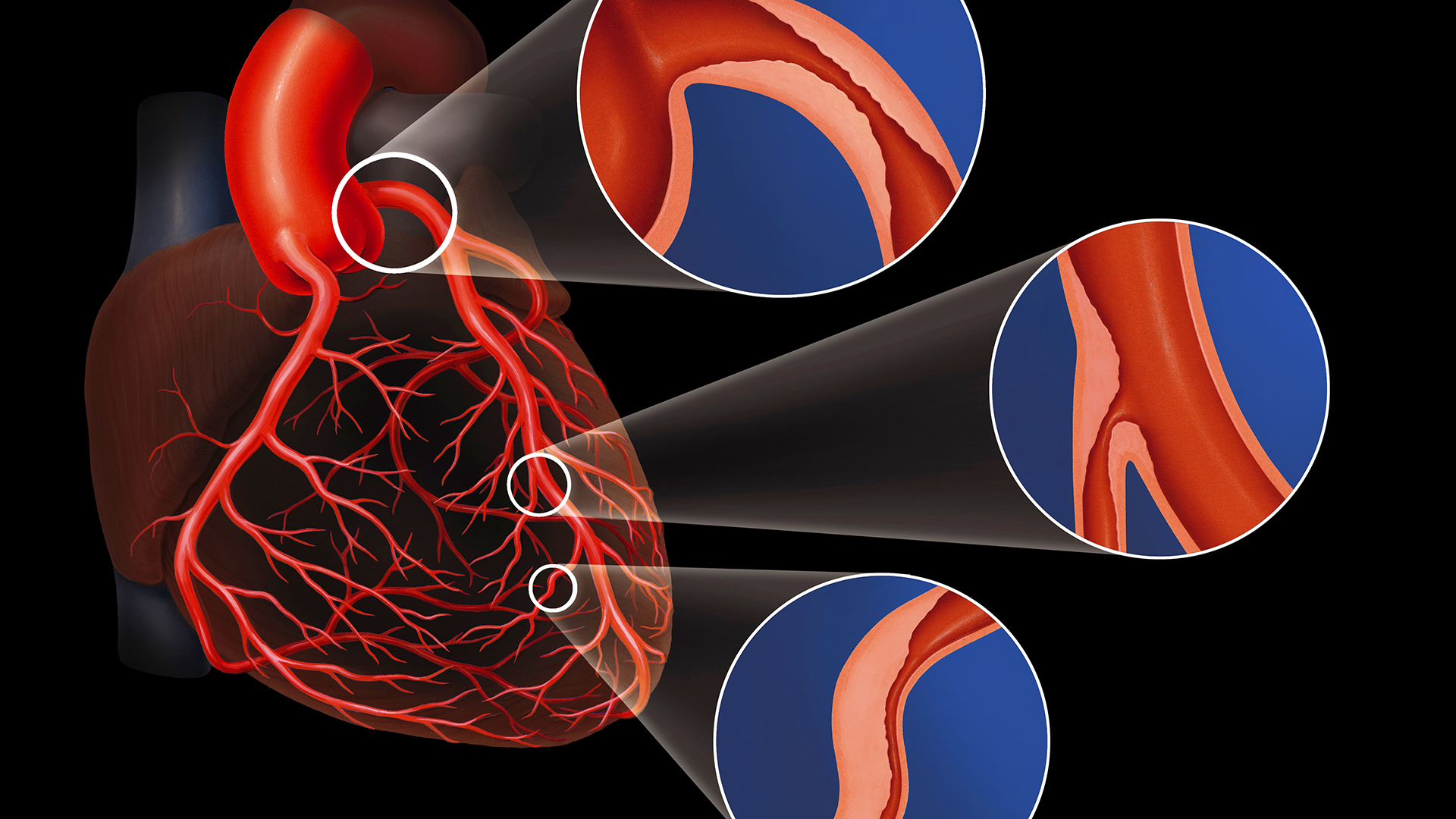
Cette thérapie non invasive trans-thoracique appelée Non-Invasive Ultrasound Therapy ou NIUT délivre précisément et de manière contrôlée de courtes impulsions ultrasonores focalisées, de haute amplitude de pression acoustique. Cela provoque un assouplissement mécanique de la valve aortique calcifiée, améliorant ainsi son ouverture et permettant à nouveau au sang oxygéné d’irriguer le corps.
Cette étude clinique, de type multicentrique et prospective, avait pour but d’évaluer la sécurité, la faisabilité et les performances de l’appareil Valvosoft.
Dix patients atteints de sténose aortique calcifiée symptomatique sévère et non éligibles pour le remplacement de la valve ont été inclus. Le dispositif Valvosoft, couplé à une sonde échocardiographique pour la surveillance en temps réel du traitement transthoracique, a délivré les ultrasons focalisés pour une durée maximale de 60 minutes. Les évaluations cliniques et échocardiographiques ont été réalisées avant thérapie et après un suivi de 30 jours, avec analyse indépendante par un laboratoire central.
Les patients avaient en moyenne 84.1 ans (± 6.5 ans), présentaient des comorbidités importantes (80% en insuffisance cardiaque et 50% avec coronaropathies) et étaient porteurs d’une sténose aortique sévère (surface moyenne de valve aortique : 0.61 ± 0.18 cm2).
Le temps moyen de traitement a été de 52 minutes. Aucun événement défavorable ne s’est produit pendant la procédure autre que des extrasystoles ventriculaires isolées. Pendant le suivi d’un mois, un patient a été hospitalisé pour insuffisance cardiaque droite qui s’est résolue. Aucun autre événement indésirable grave ne s’est produit au cours de cette période de suivi.
À un mois, un groupe de six patients, qualifiés de répondeurs*, a montré une augmentation de la surface valvulaire de 27. 6% (p = 0,031) et une diminution du gradient moyen (mean pressure gradient, p= 0.03) de 23. 5%. Ces patients avaient reçu la combinaison de la durée de thérapie et de l’énergie d’ultrason délivrée la plus élevée (>180 J/mm2 pendant au moins 45 minutes).
Aucun décès, aucun événement indésirable majeur lié au dispositif ou à la procédure, ni aucune détérioration de l’état neurologique n’ont été observés à un mois de suivi pour les 10 patients.
La faisabilité de la thérapie par ultrasons non invasive a été démontrée sur cette petite cohorte de patients atteints de sténose calcifiée sévère.
Malgré le degré de sténose très sévère des patients inclus dans cette étude préliminaire, les patients avec le temps de traitement le plus long et la dose la plus élevée ont montré des résultats cliniques et hémodynamiques prometteurs. D’autres études avec un traitement optimisé et un suivi plus long sont en cours afin d’évaluer l’innocuité et l’efficacité de cette nouvelle technique et déterminer ainsi la population qui en profitera le plus.
Référence : Feasibility and Performance of Noninvasive Ultrasound Therapy in Patients With Severe Symptomatic Aortic Valve Stenosis. A First-in-Human Study
DOI : https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.120.050672
Ce projet a été soutenu par le Programme d’Investissements d’Avenir dans le cadre du Concours Mondial de l’Innovation. Il a également bénéficié d’une aide de l’État gérée par l’Agence Nationale de la Recherche au titre du programme d’Investissements d’Avenir portant les références ANR- 16-RHUS-0003_STOP-AS et ANR-17-CE19-0019-03. Ce projet a enfin reçu le financement du programme de recherche et d’innovation Horizon 2020 de l’Union Européenne au titre de l’agrément n° 829492.
*Ont été qualifiés de répondeurs les patients pour lesquels ont été observés une amélioration de leurs paramètres hémodynamiques et anatomiques, ainsi que de leur qualité de vie.
À lire aussi

L’Université Paris Cité à l’honneur pour la 75ème édition des Lindau Nobel Laureate Meetings
Pour cette édition 2026, trois jeunes talents de l’Université Paris Cité ont été sélectionnés pour participer aux prestigieux Lindau Nobel Laureate Meetings à Lindau en Allemagne. Une opportunité unique pour Federica Namor, Marie Robert et Luca Ferrini d’échanger avec...

Chronobridge et REGolution, deux projets lauréats de l’appel MSCA-Doctoral Network 2025
Cette année, l’Université Paris Cité félicite Raphaël Porcher, Professeur de biostatistique à l’Université Paris Cité au sein du CRESS1 et partenaire du projet REGolution, ainsi que Ganna Panasyuk, Directrice de recherche à l’INEM2 et partenaire du projet...
![[Paris-NUS] Résultats des appels à projets 2026](https://u-paris.fr/wp-content/uploads/2026/04/2017-BTC-Signage-3-V2-2-1-1080x675.jpg)
[Paris-NUS] Résultats des appels à projets 2026
Dans le cadre du partenariat privilégié entre l’Université Paris Cité (UPCité) et la National University of Singapore (NUS), trois appels à projets ont été lancés en 2025, permettant aux communautés des deux établissements de renforcer et d'approfondir leurs liens. La...

