Dans ses très récents travaux, l’équipe de recherche Médecine Translationnelle et Thérapies Ciblées, dirigée par le professeur Guillaume Canaud à l’Institut Necker-Enfants Malades (Université Paris Cité, AP-HP, Inserm), vient de démontrer l’efficacité de l’alpelisib pour prévenir et améliorer la croissance du tissu adipeux des patients atteints du syndrome de surcroissance et pour inverser les anomalies métabolomiques, à la fois dans les modèles pré-cliniques et chez les patients. Cette découverte s’inscrit dans la poursuite des travaux de l’équipe qui avaient conduit, au printemps dernier, la FDA[1] à autoriser le repositionnement de l’alpelisib, médicament anticancéreux, dans ce syndrome.
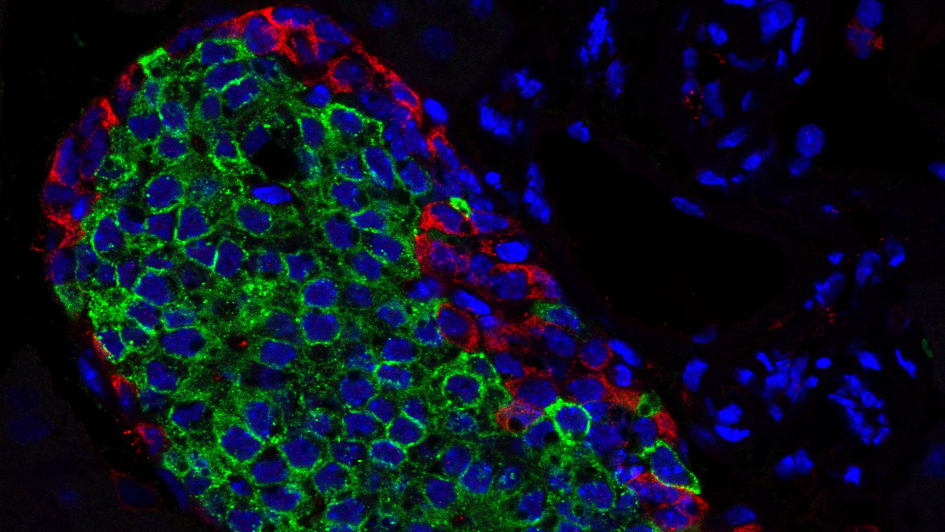
© Guillaume Canaud et Sophia Ladraa – Institut Necker-Enfants Malades (Université Paris Cité, AP-HP, Inserm)
Le syndrome de surcroissance, au cœur des travaux conduit par l’équipe du Pr Guillaume Canaud à l’Institut Necker-Enfants Malades, est dû à la mutation du gène PIK3CA, mutation qui provoque un excès de prolifération de cellules et de tissus dans l’organisme. Ces mutations, dites somatiques mosaïques, sont présentes uniquement dans les tissus et non dans le sang, ce qui les rend non-transmissibles.
Dans les précédents travaux de l’équipe, le modèle pré-clinique utilisé permettait de reproduire le syndrome de Cloves dans lequel plusieurs tissus sont affectés par cette mutation. Les études conduites avaient alors permis de démontrer l’efficacité de l’alpelisib, médicament initialement indiqué dans le traitement de certaines formes de cancers du sein, et qui a induit chez ces patients une amélioration notable de l’ensemble des paramètres cliniques, biologiques ou encore radiologiques.
Désormais et parce que de plus en plus de patients sont traités, l’équipe progresse dans la compréhension des mécanismes en jeu dans cette maladie qui se traduit par des présentations cliniques très diverses de ces mutations du gène PIK3CA. Certains patients présentent en effet plus de malformations veineuses, pour d’autres ce sont les tissus osseux les plus affectés, pour d’autres encore ce sont les tissus musculaires… L’équipe s’applique, depuis près de 3 ans, à étudier les différentes mutations du gène PIK3CA à l’origine de ces différentes malformations dans chaque type de tissus et à tester l’efficacité de ce traitement dans chaque cas. Pour ce faire, ils créent des modèles pré-cliniques spécifiques de ces différentes mutations qu’ils examinent indépendamment les unes des autres afin de mieux caractériser cette pathologie multiforme. Si différents tissus peuvent être affectés, il s’avère que le tissu adipeux est fréquemment impliqué (hypertrophies graisseuses) et que cela s’accompagne souvent de perturbations endocriniennes et métaboliques.
Les chercheurs se sont donc attachés à étudier les mécanismes en jeu dans le développement et la progression de la maladie lorsqu’elle est liée à des mutations du gène PIK3CA dans les cellules graisseuses. Ils avaient constaté chez les patients un phénomène anormal et jusque-là inexpliqué : la coexistence contradictoire d’un très faible taux de sucre dans le sang (hypoglycémie) associé à un taux d’insuline[2] lui aussi extrêmement faible. Leurs investigations leur permettent aujourd’hui d’expliquer les mécanismes moléculaires à l’origine de ce phénomène : la mutation du gène PIK3CA dans les cellules graisseuses provoque une ouverture permanente des canaux permettant le passage du sucre vers les cellules. Le sucre s’accumulant dans les cellules graisseuses, son taux dans le sang s’effondre ce qui engendre, de façon logique cette fois, un effondrement du taux d’insuline dans le sang.
Leurs travaux ont aussi permis de mettre en évidence que la mutation de PIK3CA modifie également le métabolisme des cellules graisseuses, qui se comportent, avec un effet de type Warburg, de manière similaire aux cellules cancéreuses. Ces cellules graisseuses produisent une quantité importante de lactate qu’elles utilisent ensuite pour auto-entretenir leur prolifération et leur croissance cellulaire. La suite de leurs travaux a conduit les chercheurs à tester l’efficacité de l’alpelisib sur les malformations graisseuses. Les résultats sont particulièrement encourageants puisque, chez les patients traités, l’alpelisib prouve son efficacité à plusieurs niveaux : diminution des malformations graisseuses, diminution des perturbations endocriniennes et modification du métabolisme des cellules graisseuses qui se traduit par une diminution de l’effet de type Warburg et donc une diminution de leur prolifération. L’équipe de recherche a identifié plusieurs marqueurs dans le sang qui permettent de suivre l’évolution de cet effet Warburg et de déterminer à quel moment le patient commence à répondre favorablement au traitement.
L’équipe du professeur Guillaume Canaud finalise actuellement ses travaux sur l’ensemble des autres tissus affectés par cette mutation du gène PIK3CA et devrait, dans les mois qui viennent, pouvoir évaluer de façon précise les formes de cette maladie répondant bien au traitement par l’alpelisib.
L’ensemble de ces travaux a bénéficié des soutiens financiers du Fonds de dotation Emmanuel BOUSSARD (Paris, France), European Research Council (CoG 2020 grant number 101000948), Agence Nationale de la Recherche—Programme d’Investissements d’Avenir (ANR-18-RHUS-005 to G.C.), Agence Nationale de la Recherche—Programme de Recherche Collaborative (19-CE14-0030-01 to G.C.). CLOVES Syndrome Community (West Kennebunk, USA), Association Syndrome de CLOVES (Nantes, France), Fondation d’entreprise IRCEM (Roubaix, France), Fondation DAY SOLVAY (Paris, France), Fondation TOURRE (Paris, France), Fondation BETTENCOURT SCHUELLER (Paris, France), Fondation Simone et Cino DEL DUCA (Paris, France), Fondation Line RENAUD-Loulou GASTE (Paris, France), Fondation Schlumberger pour l’Éducation et la Recherche (Paris, France), Association Robert Debré pour la Recherche Médicale, WonderFIL smiles—A Facial Infiltrating Lipomatosis community (Norway), INSERM, Assistance Publique Hôpitaux de Paris, l’Université Paris Cité
[1] Food and Drug Administration (Agence fédérale américaine des produits alimentaires et médicamenteux)
[2] L’insuline est l’hormone qui permet de réguler le taux de sucre dans le sang. Son taux est d’autant plus élevé que le taux de sucre l’est également.
Références
PIK3CA gain-of-function mutation in adipose tissue induces metabolic reprogramming with Warburg-like effect and severe endocrine disruption
Chercheurs
-
Guillaume Canaud, PU-PH, directeur de l’Unité de Médecine Translationnelle et Thérapies Ciblées
-
Sophia Ladraa, Ingénieur d’Études au sein de l’Unité de Médecine Translationnelle et Thérapies Ciblées
À lire aussi

L’Académie Spatiale d’Île-de-France lance sa première édition de la Space Executive School of Ile-de-France
Du 6 au 10 juillet 2026, l’Académie Spatiale d’île de France dont l’Université Paris Cité est partenaire, organise une semaine autour de la thématique « un spatial raisonnable pour un monde en crise climatique ». Dans ce cadre, un appel à candidature est lancé auprès...
La communauté mondiale de mycologie médicale appelle à lutter contre les champignons résistants aux médicaments
De plus en plus de champignons deviennent résistants aux traitements antifongiques, compliquant la prise en charge des patientes et patients les plus fragiles. Dans un appel publié dans Nature Medicine en mai 2026, cinquante chercheuses et chercheurs du monde entier...

Le Pr Hugues de Thé récompensé par le prestigieux prix Shaw 2026
Hugues de Thé, professeur au Collège de France et directeur de l'Institut de la Leucémie (UPCité/AP-HP/Inserm/Collège de France), est lauréat du prestigieux prix Shaw 2026 pour les sciences biologiques et médicales, aux côtés d’Anne Dejean, professeure émérite à...

IUF 2026 : l’Université Paris Cité félicite ses 11 lauréates et lauréats
Cette année, 11 enseignantes-chercheures et enseignants-chercheurs d’UPCité ont été nommés membres de l’Institut Universitaire de France (IUF). À compter du 1er octobre 2026, et pour une durée de cinq ans, les 3 chaires juniors et 8 chaires seniors offriront aux...
